フィンテプラ内用液2.2mg/mL
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
- 収載区分
- 銘柄別収載
- 先発・後発情報
- 先発品(後発品なし)
- オーソライズド
ジェネリック - -
- 一般名
- フェンフルラミン塩酸塩液
- 英名(商品名)
- Fintepla
- 規格
- 0.22%1mL
- 薬価
- 1,407.60
- メーカー名
- ユーシービージャパン/日本新薬
- 規制区分
- 劇薬
- 長期投与制限
- -
- 標榜薬効
- 抗てんかん薬〔セロトニン受容体(5−HT1D/2A/2C)作動薬〕
- 色
- 無色澄明
- 識別コード
- -
- [@: メーカーロゴ]
- 添付文書
-
PDF 2024年3月改訂(第4版)
- 告示日
- 2022年11月15日
- 経過措置期限
- -
- 医薬品マスタに反映
- 2022年12月版
- DIRに反映
- 2022年12月版
- DIR削除予定
- -
- 運転注意
-
注意情報あり(使用の適否を判断するものではありません)注意
- ドーピング
-
禁止物質あり(使用の適否を判断するものではありません)
競技会区分:競技会において禁止
セクション:S6. 興奮剤
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
効能効果
他の抗てんかん薬で十分な効果が認められない次記の患者におけるてんかん発作に対する抗てんかん薬との併用療法:1)Dravet症候群、2)Lennox-Gastaut症候群。
用法用量
〈Dravet症候群〉
(1). スチリペントールを併用する場合
通常、成人及び2歳以上の小児には、フェンフルラミンとして1日0.2mg/kgを1日2回に分けて経口投与する。なお、症状により1日0.4mg/kgを超えない範囲で適宜増減するが、増量は1週間以上の間隔をあけて行うこと。また、1日用量として17mgを超えないこと。
(2). スチリペントールを併用しない場合
通常、成人及び2歳以上の小児には、フェンフルラミンとして1日0.2mg/kgを1日2回に分けて経口投与する。なお、症状により1日0.7mg/kgを超えない範囲で適宜増減するが、増量は1週間以上の間隔をあけて行うこと。また、1日用量として26mgを超えないこと。
〈Lennox-Gastaut症候群〉
通常、成人及び2歳以上の小児には、フェンフルラミンとして1日0.2mg/kgを開始用量として1日2回に分けて経口投与し、患者の状態に応じて、1週間以上の間隔をあけて1日0.7mg/kgまで増量できる。1日用量として26mgを超えないこと。
(用法及び用量に関連する注意)
7.1. 〈Dravet症候群〉患者の状態に応じて、増量する場合には、次の漸増スケジュールを参考に、増量すること〔10.2、16.7.1参照〕。
[本剤の推奨漸増スケジュール]
1). 〈Dravet症候群〉スチリペントールを併用する場合*
①. 〈Dravet症候群〉初回投与(0日目):用量0.1mg/kg1日2回、1日最大投与量17mg。
②. 〈Dravet症候群〉7日目:用量0.15mg/kg1日2回、1日最大投与量17mg。
③. 〈Dravet症候群〉14日目:用量0.2mg/kg1日2回、1日最大投与量17mg。
2). 〈Dravet症候群〉スチリペントールを併用しない場合※
①. 〈Dravet症候群〉初回投与(0日目):用量0.1mg/kg1日2回、1日最大投与量26mg。
②. 〈Dravet症候群〉7日目:用量0.2mg/kg1日2回、1日最大投与量26mg。
③. 〈Dravet症候群〉14日目:用量0.35mg/kg1日2回、1日最大投与量26mg。
*)〈Dravet症候群〉スチリペントールはクロバザム及びバルプロ酸と併用。
※)〈Dravet症候群〉スチリペントールを併用しない場合で、より急速な増量が必要な場合は、4日ごとに増量してもよい。
7.2. 〈Lennox-Gastaut症候群〉患者の状態に応じて、増量する場合には、次の漸増スケジュールを参考に、増量すること。
[本剤の推奨漸増スケジュール*]
1). 〈Lennox-Gastaut症候群〉初回投与(0日目):用量0.1mg/kg1日2回、1日最大投与量26mg。
2). 〈Lennox-Gastaut症候群〉7日目:用量0.2mg/kg1日2回、1日最大投与量26mg。
3). 〈Lennox-Gastaut症候群〉14日目:用量0.35mg/kg1日2回、1日最大投与量26mg。
*)〈Lennox-Gastaut症候群〉より急速な増量が必要な場合は、4日ごとに増量してもよい。
7.3. 〈効能共通〉本剤の投与量は必要最小限となるよう、患者ごとに慎重に観察しながら調節すること。
7.4. 〈効能共通〉重度肝機能障害のある患者(Child-Pugh分類C)には、本剤の投与量を減量することが推奨される(これらの患者の最大推奨維持用量は1日0.4mg/kgを1日2回に分けて、ただし、1日最大投与量は17mgとする)〔9.3肝機能障害患者の項、16.6.2参照〕。
改訂情報
2024年5月22日 DSU No.326 【その他】
【6.用法及び用量】(追記)
【新様式】
〈Lennox-Gastaut症候群〉
通常、成人及び2歳以上の小児には、フェンフルラミンとして1日0.2mg/kgを開始用量として1日2回に分けて経口投与し、患者の状態に応じて、1週間以上の間隔をあけて1日0.7mg/kgまで増量できる。1日用量として26mgを超えないこと。
【7.用法及び用量に関連する注意】(追記)
【新様式】
〈Lennox-Gastaut症候群〉
患者の状態に応じて、増量する場合には、以下の漸増スケジュールを参考に、増量すること。
本剤の推奨漸増スケジュール注3)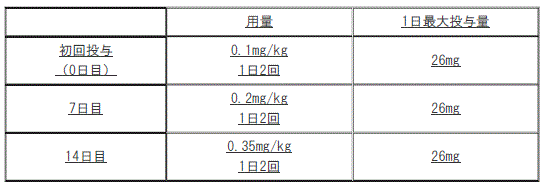
注3)より急速な増量が必要な場合は、4日ごとに増量してもよい
【7.用法及び用量に関連する注意】(一部改訂)
【新様式】
〈効能共通〉
重度の肝機能障害のある患者(Child-Pugh分類C)には、本剤の投与量を減量することが推奨される。これらの患者の最大推奨維持用量は1日0.4mg/kgを1日2回に分けて、ただし、1日最大投与量は17mgとする。
【9.1合併症・既往歴等のある患者】(一部改訂)
【新様式】
閉塞隅角緑内障患者:
閉塞隅角緑内障の前兆となる瞳孔散大がみられることがある。治療開始前に、光輪、視野ぼやけ、眼痛の既往歴について患者に確認すること。
【10.2併用注意】(一部改訂)
【新様式】
【11.2その他の副作用】(一部改訂)
【新様式】
注)病的な逆流所見ではない
【13.過量投与】(一部改訂)
【新様式】
[症状]
激越、傾眠状態、錯乱、潮紅、振戦(又は戦慄)、発熱、発汗、腹痛、過換気及び散大した非反応性瞳孔が報告されている。
よく一緒に見られている薬
医師の処方により使用する医薬品。
特定薬剤管理指導加算等の算定対象となる薬剤。


