「薬の検索」は、下記の内容に同意いただいた上でご利用ください。
禁止事項
- 掲載された情報の一括大量ダウンロード
- 許可無くコンテンツの一部または全部を流用したコンテンツの作成
- PDFファイルや画像ファイルへのリンク
注意事項
- 本サービスでは最新情報を提供するよう努力致しますが、医薬品の情報は随時更新されるため、すべての情報が最新とは限らず、その正確性および完全性等に関してはいかなる保証もするものではありません。最新情報については、各製薬メーカー、厚生労働省、医薬品医療機器総合機構が提供する情報を適宜ご参照ください。
- 本サービスの情報をもとにご自身の判断で薬の使用や中止をするようなことはせず、必ず医師や薬剤師にご相談ください。
- 添付文書情報が未入手の薬品もございますので、予めご了承ください。
- 運転注意対象薬の検索結果は、薬の使用の適否を判断するものではありません。必ず担当の医師や薬剤師にご相談ください。
- ドーピング対象薬の検索結果は、薬の使用の適否を判断するものではありません。薬を使用する際は、必ず医師や薬剤師、各競技団体等にご相談ください。
- ドーピング対象薬検索は医薬品の有効成分を対象としており、添加物は対象外です。
- OTC医薬品は医薬品の有効成分を対象としており、添加物は対象外です。
- OTC医薬品は医師の処方がなくても購入できますが、症状の悪化、副作用・事故等を防ぐために、必ず添付文書をよく読み、指示に従って使用してください。
ご利用条件
このWebサイト(以下、当サイト)は、データインデックス株式会社(以下、当社)により開設、運営されています。
ご利用に先立ち、下記のご利用条件をご熟読いただきたく、お願い申し上げます。なお、一旦ご利用を開始されました後は、下記のご利用条件および関連するすべての法律の遵守いただくことをご承諾いただいたものとみなします。
著作権について
当サイトに含まれるすべての内容は、当社および当該内容提供者の財産であり、各国の著作権法、各種条約およびその他の法律によって保護されております。当サイトの利用は、非営利目的の個人的利用の範囲内に限るものとし、この範囲を超えてのダウンロード、複製等一切の利用を禁じます。また、いかなる場合においても、内容に変更を加えたり、更なる複製を行うことを禁じます。
商標等について
当サイトに表示されている商標、ロゴマーク、商号等は法的に保護されています。これらの無断使用などの侵害行為を禁じます。
免責事項
当サイトに掲載する情報に関して細心の注意を払っておりますが、その内容の正確性・有用性・完全性、およびエラー・ウィルス感染等の危険がないことの安全性等のいずれについても保証するものではなく、いかなる責任を負うものでもありません。また、当サイトないしは当サイトに掲載された情報を利用されたこと、または利用できなかったことにより生じるいかなる損害についても何ら責任を負いません。また、予告なしに当サイトに掲載する情報の内容を変更したり、サイトを閉鎖させていただくことがありますので、予めご了承ください。
医療情報について
当サイトに掲載されている医療情報は、一般的な情報提供を目的としており、決して医師その他医療従事者によるアドバイスの代替となるものではありません。
また、当サイトに掲載されている医薬品に関する情報は、日本における医薬品添付文書の情報をもとに作成しており、日本以外の国での利用においては、これらの情報が適切でない場合がありますので、それぞれの国における承認の有無や承認内容をご確認ください。
なお、当サイトに掲載されている医薬品に関する情報は、その製品の効能・効果を宣伝または広告するものではありません。
ブラウザの推奨環境について
当サイトのコンテンツを快適にご利用いただくために、下記のWebブラウザでご覧いただくことを推奨致します。環境が満たされていない場合、各種コンテンツを正しくご利用いただけない場合がございます。
PC:Microsoft Edge、Mozilla Firefox、Safari、Google Chrome 各最新(推奨画面サイズ:横幅 1024px以上)
スマートフォン:Safari、Google Chrome 各最新
iPhone:OS14以上、Android:OS9以上
アクセス情報の取得について
当サイトでは、サービスの利便性向上を目的として、個人の特定が可能な情報を除いた範囲でCookieやアクセスログを利用して、利用者のアクセス情報を収集しておりますので、予めご了承ください。
電子メールによる情報について
電子メール等により利用者から一方的に提供される情報・資料に対しては、何ら返信の義務を負うものではなく、利用者の個人情報(取扱いについては別途個人情報保護方針で規定しておりますのでご参照ください)を除き、機密の取扱いを致しかねます。また、当社は、個人情報を除いた当該情報・資料をいかなる目的にも無償で自由に利用できるものとします。
リンクについて
当サイトへのリンクをご希望の場合は、事前に当社へご連絡いただき承諾を得てください。また、当サイトにリンクしている第三者のWebサイト、または当サイトがリンクを設けている第三者のWebサイトについては、一切の責任を負いません。
ご連絡は、お問い合わせ等をご利用ください。
雑誌などへの掲載について
雑誌書籍、広告などの出版物等の各種メディアへの掲載を希望される場合は、事前に当社へご連絡いただき承諾を得てください。
ご連絡は、お問い合わせ等をご利用ください。
英語サイトについて
英語サイトの内容は、原則として日本語サイトに掲載された原文の翻訳とし、日本語サイトの原文と英語サイトの翻訳に齟齬がある場合は、日本語の原文の内容を優先します。
その他
この利用条件は、日本法を準拠法とし、それに基づいて解釈されるものとします。この利用条件に関わるすべての紛争については、東京地方裁判所を第一審の専属的管轄裁判所とするものとします。
ボリコナゾール錠200mg「NIG」
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
医薬品コード(YJコード):6179001F2119
- 収載区分
- 銘柄別収載
- 先発・後発情報
- 後発品(加算対象)
- オーソライズド
ジェネリック - -
- 一般名
- ボリコナゾール錠
- 英名(商品名)
- Voriconazole
- 規格
- 200mg1錠
- 薬価
- 513.80
- メーカー名
- 日医工岐阜工場/日医工/武田薬品
- 規制区分
- 劇薬
- 長期投与制限
- -
- 標榜薬効
- 抗真菌薬〔トリアゾール系抗菌薬〕
- 色
- 白
- 識別コード
- (本体)TV VZ2 (本体)200 (被包)200 TV VZ2
- [@: メーカーロゴ]
- 添付文書
-
PDF 2024年11月改訂(第4版)
- 告示日
- 2022年12月8日
- 経過措置期限
- -
- 医薬品マスタに反映
- 2023年1月版
- 医薬品マスタ削除予定
- -
- 運転注意
-
禁止情報あり(使用の適否を判断するものではありません)禁止
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
効能効果
1). 次記の重症又は難治性真菌感染症:
・ 侵襲性アスペルギルス症、肺アスペルギローマ、慢性壊死性肺アスペルギルス症。
・ カンジダ血症、食道カンジダ症、カンジダ腹膜炎、気管支カンジダ症・肺カンジダ症。
・ クリプトコックス髄膜炎、肺クリプトコックス症。
・ フサリウム症。
・ スケドスポリウム症。
2). 造血幹細胞移植患者における深在性真菌症の予防。
(効能又は効果に関連する注意)
5.1. 〈カンジダ感染の治療〉他の抗真菌剤が無効あるいは忍容性に問題があると考えられる場合に本剤の使用を考慮すること。
5.2. 〈造血幹細胞移植患者における深在性真菌症の予防〉真菌感染に高リスクの患者(好中球数が500/mm3未満に減少することが予測される患者など)を対象とすること。
用法用量
1). 成人(体重40kg以上):通常、ボリコナゾールとして初日は1回300mgを1日2回、2日目以降は1回150mg又は1回200mgを1日2回食間に経口投与する。なお、患者の状態に応じて、又は効果不十分の場合には、増量できるが、初日投与量の上限は1回400mg1日2回、2日目以降投与量の上限は1回300mg1日2回までとする。
2). 成人(体重40kg未満):通常、ボリコナゾールとして初日は1回150mgを1日2回、2日目以降は1回100mgを1日2回食間に経口投与する。なお、患者の状態に応じて、又は効果不十分の場合には2日目以降の投与量を1回150mg1日2回まで増量できる。
3). 小児(2歳以上12歳未満及び12歳以上で体重50kg未満):ボリコナゾール注射剤による投与を行った後、通常、ボリコナゾールとして1回9mg/kgを1日2回食間に経口投与する。なお、患者の状態に応じて、又は効果不十分の場合には1mg/kgずつ増量し、忍容性が不十分の場合には1mg/kgずつ減量する(最大投与量として350mgを用いた場合は50mgずつ減量する)。
ただし、1回350mg1日2回を上限とする。
4). 小児(12歳以上で体重50kg以上):ボリコナゾール注射剤による投与を行った後、通常、ボリコナゾールとして1回200mgを1日2回食間に経口投与する。なお、患者の状態に応じて、又は効果不十分の場合には1回300mg1日2回まで増量できる。
(用法及び用量に関連する注意)
7.1. 〈効能共通〉注射剤からボリコナゾールの投与を開始した成人患者において、経口投与可能であると医師が判断した場合は、錠剤又はドライシロップに切り替えることができる。
7.2. 〈効能共通〉小児においては、注射剤からボリコナゾールの投与を開始し、患者の状態に応じて、経口投与可能であると医師が判断した場合に、錠剤又はドライシロップに切り替えることができるが、投与開始から1週間未満で注射剤から経口剤に変更した際の有効性及び安全性は検討されていないため慎重に判断すること。なお、ボリコナゾール注射剤では食道カンジダ症の適応はないため、小児の食道カンジダ症に対する本剤の使用は推奨されない〔16.1.2参照〕。
7.3. 〈効能共通〉腎機能障害のある患者で注射剤の投与ができない成人患者に対しては、錠剤又はドライシロップを使用すること。
7.4. 〈効能共通〉軽度~中等度肝機能低下(Child Pugh分類クラスA・Bの肝硬変に相当)がある患者では投与初日は通常の初日投与量とし、2日目以降は通常の2日目以降投与量の半量とすること〔9.3.2、15.1.1、16.6.1参照〕。
7.5. 〈造血幹細胞移植患者における深在性真菌症の予防〉好中球数が500/mm3以上に回復する、又は免疫抑制剤の投与終了など、適切な時期に投与を終了すること(臨床試験において、180日を超えた投与の有効性及び安全性は検討されていない)。
外形画像



改訂情報
2024年11月27日 DSU No.331 【重要】
【8.重要な基本的注意】(一部改訂)
重篤な血液障害、重篤な腎障害、高カリウム血症があらわれることがあるので、本剤の投与に際しては定期的に血液検査、腎機能検査、血中電解質検査を行うなど観察を十分に行うこと。
【11.1重大な副作用】(追記)
高カリウム血症
2024年11月27日 DSU No.331 【その他】
【11.2その他の副作用】(削除)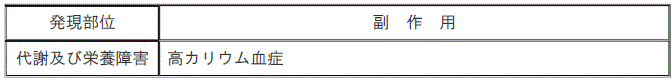
2024年11月13日 使用上の注意改訂情報 令和6年11月13日指示分
【8. 重要な基本的注意】(一部改訂)
重篤な血液障害、重篤な腎障害、高カリウム血症があらわれることがあるので、本剤の投与に際しては定期的に血液検査、腎機能検査、血中電解質検査を行うなど観察を十分に行うこと。
【11. 副作用-11.1 重大な副作用】(新設)
高カリウム血症
2024年6月25日 DSU No.327 【重要】
【2.禁忌】(一部改訂)
次の薬剤を投与中の患者:リファンピシン、リファブチン、エファビレンツ、リトナビル、ロピナビル・リトナビル、ニルマトレルビル・リトナビル、カルバマゼピン、バルビタール、フェノバルビタール、ピモジド、キニジン、イバブラジン、麦角アルカロイド(エルゴタミン・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン)、トリアゾラム、チカグレロル、アスナプレビル、ロミタピド、ブロナンセリン、スボレキサント、リバーロキサバン、リオシグアト、アゼルニジピン、オルメサルタンメドキソミル・アゼルニジピン、ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)、アナモレリン、ルラシドン、イサブコナゾニウム、フィネレノン
【10.1併用禁忌】(追記)
2024年6月11日 使用上の注意改訂情報 令和6年6月11日指示分
【2. 禁忌(次の患者には投与しないこと)】(一部改訂)
【新記載要領】
次の薬剤を投与中の患者:リファンピシン、リファブチン、エファビレンツ、リトナビル、ロピナビル・リトナビル、ニルマトレルビル・リトナビル、カルバマゼピン、バルビタール、フェノバルビタール、ピモジド、キニジン、イバブラジン、麦角アルカロイド(エルゴタミン・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン)、トリアゾラム、チカグレロル、アスナプレビル、ロミタピド、ブロナンセリン、スボレキサント、リバーロキサバン、リオシグアト、アゼルニジピン、オルメサルタン メドキソミル・アゼルニジピン、ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)、アナモレリン、ルラシドン、イサブコナゾニウム、フィネレノン
【10. 相互作用-10.1 併用禁忌(併用しないこと)】(新設)
【新記載要領】
医師の処方により使用する医薬品。



 で医薬品を比較する
で医薬品を比較する
