イグザレルト細粒分包15mg
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
- 収載区分
- 銘柄別収載
- 先発・後発情報
- 先発品(後発品なし)
- オーソライズド
ジェネリック - -
- 一般名
- リバーロキサバン細粒
- 英名(商品名)
- Xarelto
- 規格
- 15mg1包
- 薬価
- 521.40
- メーカー名
- バイエル薬品
- 規制区分
- -
- 長期投与制限
- -
- 標榜薬効
- 血液凝固第10a因子(F10a)阻害薬
- 色
- 白
- 識別コード
- (被包)@ Xarelto Fine Granules (被包)BAYER Xarelto Fine Granules
- [@: メーカーロゴ]
- 添付文書
-
PDF 2024年11月改訂(第8版)
- 告示日
- 2015年11月27日
- 経過措置期限
- -
- 医薬品マスタに反映
- 2015年12月版
- 医薬品マスタ削除予定
- -
- 運転注意
- 情報なし(使用の適否を判断するものではありません)
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
効能効果
1). 成人:
①. 非弁膜症性心房細動患者における虚血性脳卒中及び全身性塞栓症の発症抑制。
②. 静脈血栓塞栓症(深部静脈血栓症及び肺血栓塞栓症)の治療及び再発抑制。
2). 小児:
①. 静脈血栓塞栓症の治療及び再発抑制。
②. Fontan手術施行後における血栓・塞栓形成の抑制。
(効能又は効果に関連する注意)
5.1. 〈静脈血栓塞栓症の治療及び再発抑制〉成人のショックや低血圧が遷延するような血行動態が不安定な肺血栓塞栓症患者、若しくは成人の血栓溶解療法が必要な肺血栓塞栓症又は成人の肺塞栓摘除術が必要な肺血栓塞栓症患者に対する本剤の安全性及び有効性は検討されていないので、これらの患者に対してヘパリンの代替療法として本剤を投与しないこと。
5.2. 〈静脈血栓塞栓症の治療及び再発抑制〉静脈血栓塞栓症の治療及び再発抑制の場合、小児では、本剤は急性期への適切な初期治療(ヘパリン投与等)が5日以上なされた後に投与すること。
5.3. 〈静脈血栓塞栓症の治療及び再発抑制〉下大静脈フィルターが留置された患者に対する本剤の安全性及び有効性は検討されていない。
用法用量
〈非弁膜症性心房細動患者における虚血性脳卒中及び全身性塞栓症の発症抑制〉
通常、成人にはリバーロキサバンとして15mgを1日1回食後に経口投与する。なお、腎障害のある患者に対しては、腎機能の程度に応じて10mg1日1回に減量する。
〈静脈血栓塞栓症の治療及び再発抑制〉
成人
通常、成人には深部静脈血栓症又は肺血栓塞栓症発症後の初期3週間はリバーロキサバンとして15mgを1日2回食後に経口投与し、その後は15mgを1日1回食後に経口投与する。
小児
通常、体重30kg以上の小児にはリバーロキサバンとして15mgを1日1回食後に経口投与する。
〈Fontan手術施行後における血栓・塞栓形成の抑制〉
通常、体重50kg以上の小児にはリバーロキサバンとして10mgを1日1回経口投与する。
(用法及び用量に関連する注意)
7.1. 〈非弁膜症性心房細動患者における虚血性脳卒中及び全身性塞栓症の発症抑制〉非弁膜症性心房細動でクレアチニンクリアランス30~49mL/minの患者には、10mgを1日1回投与する〔9.2.3、16.6.1、17.1.1参照〕。
7.2. 〈非弁膜症性心房細動患者における虚血性脳卒中及び全身性塞栓症の発症抑制〉非弁膜症性心房細動でクレアチニンクリアランス15~29mL/minの患者には、本剤投与の適否を慎重に検討した上で、投与する場合は、10mgを1日1回投与する〔9.2.2、16.6.1参照〕。
7.3. 〈静脈血栓塞栓症の治療及び再発抑制〉体重30kg未満の小児等に投与する場合は、リバーロキサバンドライシロップを使用すること。
7.4. 〈Fontan手術施行後における血栓・塞栓形成の抑制〉体重20kg未満の小児等に投与する場合は、リバーロキサバンドライシロップを使用し、Fontan手術施行後における血栓・塞栓形成の抑制で体重20kg以上50kg未満の小児等に投与する場合は、リバーロキサバン錠2.5mg又はドライシロップを使用すること。
改訂情報
2024年11月27日 DSU No.331 【その他】
【2.禁忌】(一部改訂)
リトナビルを含有する製剤、アタザナビル、ダルナビル、ホスアンプレナビルを投与中の患者
【2.禁忌】(一部改訂)
イトラコナゾール、ポサコナゾール、ボリコナゾール、ミコナゾール、ケトコナゾールの経口又は注射剤を投与中の患者
【10.1併用禁忌】(一部改訂)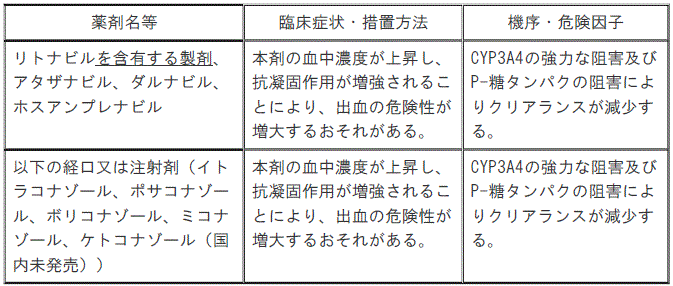
2024年5月22日 DSU No.326 【重要】
【2.禁忌】(一部改訂)
【新様式】
〈効能共通〉
アゾール系抗真菌剤(イトラコナゾール、ボリコナゾール、ミコナゾール、ポサコナゾール、ケトコナゾール)の経口又は注射剤を投与中の患者
【10.1併用禁忌】(一部改訂)
【新様式】
2024年5月22日 DSU No.326 【その他】
【10.1併用禁忌】(削除)
【新様式】
エルビテグラビル・コビシスタット・エムトリシタビン・テノホビルジソプロキシルフマル酸塩
2024年5月8日 使用上の注意改訂情報 令和6年5月8日指示分
【2. 禁忌(次の患者には投与しないこと)】(一部改訂)
【新記載要領】
〈効能共通〉
アゾール系抗真菌剤(イトラコナゾール、ボリコナゾール、ミコナゾール、ポサコナゾール、ケトコナゾール)の経口又は注射剤を投与中の患者
【10. 相互作用-10.1 併用禁忌(併用しないこと)】(一部改訂)
【新記載要領】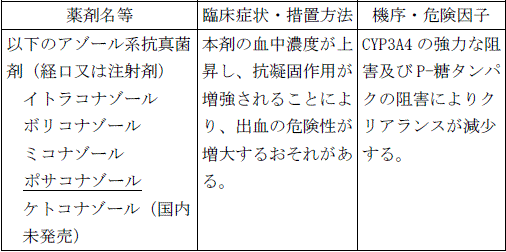
類似した薬効の薬
よく一緒に見られている薬
医師の処方により使用する医薬品。
特定薬剤管理指導加算等の算定対象となる薬剤。



 で医薬品を比較する
で医薬品を比較する
