トレプロスト吸入液1.74mg
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
医薬品コード(YJコード):2190702G1020
- 収載区分
- 銘柄別収載
- 先発・後発情報
- 先発品(後発品なし)
- オーソライズド
ジェネリック - -
- 一般名
- トレプロスチニル吸入剤
- 英名(商品名)
- Treprost
- 規格
- 1.74mg2.9mL1管
- 薬価
- 21,751.30
- メーカー名
- 持田製薬
- 規制区分
- 劇薬
- 長期投与制限
- -
- 標榜薬効
- 末梢血管拡張薬〔プロスタグランジンI2(PGI2)誘導体〕
- 色
- 無色澄明
- 識別コード
- -
- [@: メーカーロゴ]
- 添付文書
-
PDF 2025年1月改訂(第5版)
- 告示日
- 2023年3月14日
- 経過措置期限
- -
- 医薬品マスタに反映
- 2023年4月版
- 医薬品マスタ削除予定
- -
- 運転注意
-
注意情報あり(使用の適否を判断するものではありません)注意
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
効能効果
1). 肺動脈性肺高血圧症。
2). 間質性肺疾患に伴う肺高血圧症。
(効能又は効果に関連する注意)
5.1. 〈効能共通〉本剤の使用にあたっては、最新の治療ガイドラインを参考に投与の要否を検討すること。
5.2. 〈肺動脈性肺高血圧症〉肺動脈性肺高血圧症のWHO機能分類クラス1における有効性及び安全性は確立していない。
5.3. 〈肺動脈性肺高血圧症〉特発性PAH・遺伝性PAH及び結合組織病に伴うPAH以外のPAHにおける有効性及び安全性は確立していない(PAH:肺動脈性肺高血圧症)。
5.4. 〈間質性肺疾患に伴う肺高血圧症〉「17.臨床成績」の項の内容を熟知し、臨床試験に組み入れられた患者の背景(間質性肺疾患の臨床分類等)を十分に理解した上で、適応患者を選択すること。
5.5. 〈間質性肺疾患に伴う肺高血圧症〉間質性肺疾患に伴う肺高血圧症のWHO機能分類クラス4における有効性及び安全性は確立していない。
用法用量
〈肺動脈性肺高血圧症〉
通常、成人には、1日4回ネブライザを用いて吸入投与する。1回3吸入(トレプロスチニルとして18μg)から投与を開始し、忍容性を確認しながら、7日以上の間隔で、1回3吸入ずつ、最大9吸入(トレプロスチニルとして54μg)まで漸増する。3吸入の増量に対して忍容性に懸念がある場合は、増量幅を1又は2吸入としてもよい。忍容性がない場合は減量し、1回最小量は1吸入とすること。
〈間質性肺疾患に伴う肺高血圧症〉
通常、成人には、1日4回ネブライザを用いて吸入投与する。1回3吸入(トレプロスチニルとして18μg)から投与を開始し、忍容性を確認しながら、3日以上の間隔で、1回1吸入ずつ、最大12吸入(トレプロスチニルとして72μg)まで漸増する。忍容性がない場合は減量し、1回最小量は1吸入とすること。
(用法及び用量に関連する注意)
7.1. 吸入間隔は約4時間あけること。
7.2. 本剤の吸入にはTD-300/Jネブライザを使用すること〔14.1参照〕。
7.3. 肝障害のある患者においては、重症度に応じて1回1又は2吸入から投与を開始し、慎重に増量すること〔9.3肝機能障害患者の項、16.6.2参照〕。
改訂情報
2024年11月27日 DSU No.331 【その他】
【5.効能又は効果に関連する注意】(追記)
〈間質性肺疾患に伴う肺高血圧症〉
「17.臨床成績」の項の内容を熟知し、臨床試験に組み入れられた患者の背景(間質性肺疾患の臨床分類等)を十分に理解した上で、適応患者を選択すること。
【5.効能又は効果に関連する注意】(追記)
WHO機能分類クラスⅣにおける有効性及び安全性は確立していない。
【6.用法及び用量】(追記)
〈間質性肺疾患に伴う肺高血圧症〉
通常、成人には、1日4回ネブライザを用いて吸入投与する。1回3吸入(トレプロスチニルとして18μg)から投与を開始し、忍容性を確認しながら、3日以上の間隔で、1回1吸入ずつ、最大12吸入(トレプロスチニルとして72μg)まで漸増する。忍容性がない場合は減量し、1回最小量は1吸入とすること。
【9.5妊婦】(一部改訂)
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。動物実験(ウサギ)において骨格変異(腰肋骨)を有する胎児の発生率の増加が臨床曝露量(トレプロスチニルとして72μg吸入投与時)の3.1倍に相当する曝露量で認められている。
【11.2その他の副作用】(一部改訂)
2024年4月11日 DSU No.325 【その他】
【11.2その他の副作用】(一部改訂)
【新様式】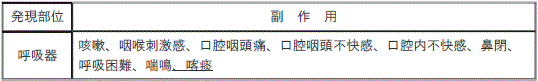
医師の処方により使用する医薬品。



 で医薬品を比較する
で医薬品を比較する
