「薬の検索」は、下記の内容に同意いただいた上でご利用ください。
禁止事項
- 掲載された情報の一括大量ダウンロード
- 許可無くコンテンツの一部または全部を流用したコンテンツの作成
- PDFファイルや画像ファイルへのリンク
注意事項
- 本サービスでは最新情報を提供するよう努力致しますが、医薬品の情報は随時更新されるため、すべての情報が最新とは限らず、その正確性および完全性等に関してはいかなる保証もするものではありません。最新情報については、各製薬メーカー、厚生労働省、医薬品医療機器総合機構が提供する情報を適宜ご参照ください。
- 本サービスの情報をもとにご自身の判断で薬の使用や中止をするようなことはせず、必ず医師や薬剤師にご相談ください。
- 添付文書情報が未入手の薬品もございますので、予めご了承ください。
- 運転注意対象薬の検索結果は、薬の使用の適否を判断するものではありません。必ず担当の医師や薬剤師にご相談ください。
- ドーピング対象薬の検索結果は、薬の使用の適否を判断するものではありません。薬を使用する際は、必ず医師や薬剤師、各競技団体等にご相談ください。
- ドーピング対象薬検索は医薬品の有効成分を対象としており、添加物は対象外です。
- OTC医薬品は医薬品の有効成分を対象としており、添加物は対象外です。
- OTC医薬品は医師の処方がなくても購入できますが、症状の悪化、副作用・事故等を防ぐために、必ず添付文書をよく読み、指示に従って使用してください。
ご利用条件
このWebサイト(以下、当サイト)は、データインデックス株式会社(以下、当社)により開設、運営されています。
ご利用に先立ち、下記のご利用条件をご熟読いただきたく、お願い申し上げます。なお、一旦ご利用を開始されました後は、下記のご利用条件および関連するすべての法律の遵守いただくことをご承諾いただいたものとみなします。
著作権について
当サイトに含まれるすべての内容は、当社および当該内容提供者の財産であり、各国の著作権法、各種条約およびその他の法律によって保護されております。当サイトの利用は、非営利目的の個人的利用の範囲内に限るものとし、この範囲を超えてのダウンロード、複製等一切の利用を禁じます。また、いかなる場合においても、内容に変更を加えたり、更なる複製を行うことを禁じます。
商標等について
当サイトに表示されている商標、ロゴマーク、商号等は法的に保護されています。これらの無断使用などの侵害行為を禁じます。
免責事項
当サイトに掲載する情報に関して細心の注意を払っておりますが、その内容の正確性・有用性・完全性、およびエラー・ウィルス感染等の危険がないことの安全性等のいずれについても保証するものではなく、いかなる責任を負うものでもありません。また、当サイトないしは当サイトに掲載された情報を利用されたこと、または利用できなかったことにより生じるいかなる損害についても何ら責任を負いません。また、予告なしに当サイトに掲載する情報の内容を変更したり、サイトを閉鎖させていただくことがありますので、予めご了承ください。
医療情報について
当サイトに掲載されている医療情報は、一般的な情報提供を目的としており、決して医師その他医療従事者によるアドバイスの代替となるものではありません。
また、当サイトに掲載されている医薬品に関する情報は、日本における医薬品添付文書の情報をもとに作成しており、日本以外の国での利用においては、これらの情報が適切でない場合がありますので、それぞれの国における承認の有無や承認内容をご確認ください。
なお、当サイトに掲載されている医薬品に関する情報は、その製品の効能・効果を宣伝または広告するものではありません。
ブラウザの推奨環境について
当サイトのコンテンツを快適にご利用いただくために、下記のWebブラウザでご覧いただくことを推奨致します。環境が満たされていない場合、各種コンテンツを正しくご利用いただけない場合がございます。
PC:Microsoft Edge、Mozilla Firefox、Safari、Google Chrome 各最新(推奨画面サイズ:横幅 1024px以上)
スマートフォン:Safari、Google Chrome 各最新
iPhone:OS14以上、Android:OS9以上
アクセス情報の取得について
当サイトでは、サービスの利便性向上を目的として、個人の特定が可能な情報を除いた範囲でCookieやアクセスログを利用して、利用者のアクセス情報を収集しておりますので、予めご了承ください。
電子メールによる情報について
電子メール等により利用者から一方的に提供される情報・資料に対しては、何ら返信の義務を負うものではなく、利用者の個人情報(取扱いについては別途個人情報保護方針で規定しておりますのでご参照ください)を除き、機密の取扱いを致しかねます。また、当社は、個人情報を除いた当該情報・資料をいかなる目的にも無償で自由に利用できるものとします。
リンクについて
当サイトへのリンクをご希望の場合は、事前に当社へご連絡いただき承諾を得てください。また、当サイトにリンクしている第三者のWebサイト、または当サイトがリンクを設けている第三者のWebサイトについては、一切の責任を負いません。
ご連絡は、お問い合わせ等をご利用ください。
雑誌などへの掲載について
雑誌書籍、広告などの出版物等の各種メディアへの掲載を希望される場合は、事前に当社へご連絡いただき承諾を得てください。
ご連絡は、お問い合わせ等をご利用ください。
英語サイトについて
英語サイトの内容は、原則として日本語サイトに掲載された原文の翻訳とし、日本語サイトの原文と英語サイトの翻訳に齟齬がある場合は、日本語の原文の内容を優先します。
その他
この利用条件は、日本法を準拠法とし、それに基づいて解釈されるものとします。この利用条件に関わるすべての紛争については、東京地方裁判所を第一審の専属的管轄裁判所とするものとします。
デュロテップMTパッチ4.2mg
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
医薬品コード(YJコード):8219700S6022
- 収載区分
- 銘柄別収載
- 先発・後発情報
- その他
- オーソライズド
ジェネリック - -
- 一般名
- フェンタニル貼付剤(2)
- 英名(商品名)
- Durotep
- 規格
- 4.2mg1枚
- 薬価
- 2,868.40
- メーカー名
- ヤンセンファーマ
- 規制区分
- 劇薬/麻薬
- 長期投与制限
- 30日
- 標榜薬効
- 麻薬性オピオイド
- 色
- 半透明
- 識別コード
- -
- [@: メーカーロゴ]
- 添付文書
-
PDF 2024年12月改訂(第3版)
- 告示日
- 2008年6月20日
- 経過措置期限
- -
- 医薬品マスタに反映
- -
- 医薬品マスタ削除予定
- -
- 運転注意
-
禁止情報あり(使用の適否を判断するものではありません)禁止
- ドーピング
-
禁止物質あり(使用の適否を判断するものではありません)
競技会区分:競技会において禁止
セクション:S7. 麻薬
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
効能効果
非オピオイド鎮痛剤及び弱オピオイド鎮痛剤で治療困難な次記疾患における鎮痛:
1). 中等度から高度の疼痛を伴う各種癌における鎮痛(ただし、他のオピオイド鎮痛剤から切り替えて使用する場合に限る)。
2). 中等度から高度の慢性疼痛における鎮痛(ただし、他のオピオイド鎮痛剤から切り替えて使用する場合に限る)。
(効能又は効果に関連する注意)
5.1. 本剤は、他のオピオイド鎮痛剤が一定期間投与され、忍容性が確認された患者で、かつオピオイド鎮痛剤の継続的な投与を必要とするがん疼痛及び慢性疼痛の管理にのみ使用すること。
5.2. 慢性疼痛の原因となる器質的病変、心理的・社会的要因、依存リスクを含めた包括的な診断を行い、本剤の投与の適否を慎重に判断すること。
用法用量
本剤は、オピオイド鎮痛剤から切り替えて使用する。
通常、成人に対し胸部、腹部、上腕部、大腿部等に貼付し、3日毎(約72時間)に貼り替えて使用する。
初回貼付用量は本剤投与前に使用していたオピオイド鎮痛剤の用法・用量を勘案して、2.1mg(12.5μg/hr)、4.2mg(25μg/hr)、8.4mg(50μg/hr)、12.6mg(75μg/hr)のいずれかの用量を選択する。
その後の貼付用量は患者の症状や状態により適宜増減する。
(用法及び用量に関連する注意)
7.1. 初回貼付用量
初回貼付用量として、本剤16.8mg(100μg/hr)は推奨されない(本邦において、初回貼付用量として12.6mg(75μg/hr)を超える使用経験はない)。
初回貼付用量を選択する換算は、経口モルヒネ量90mg/日(坐剤の場合45mg/日、注射の場合30mg/日)に対して本剤4.2mg(25μg/hr;フェンタニル0.6mg/日)へ切り替えるものとして設定、初回貼付用量を選択する換算は、経口オキシコドン量60mg/日に対して本剤4.2mg(25μg/hr;フェンタニル0.6mg/日)へ切り替えるものとして設定、初回貼付用量を選択する換算は、経口コデイン量270mg/日以上に対して本剤4.2mg(25μg/hr;フェンタニル0.6mg/日)へ切り替えるものとして設定、初回貼付用量を選択する換算は、フェンタニル経皮吸収型製剤(1日貼付型製剤)1.7mg(フェンタニル0.6mg/日)に対して本剤4.2mg(25μg/hr;フェンタニル0.6mg/日)へ切り替えるものとして設定している。
なお、初回貼付用量は換算に基づく適切な用量を選択し、過量投与にならないよう注意すること。
[換算(オピオイド鎮痛剤1日使用量に基づく推奨貼付用量):がん疼痛における切り替え]
1). モルヒネ経口剤<45mg/日:本剤3日貼付用量2.1mg、*定常状態における推定平均吸収速度12.5μg/hr、*定常状態における推定平均吸収量0.3mg/日。
2). モルヒネ経口剤45~134mg/日:本剤3日貼付用量4.2mg、*定常状態における推定平均吸収速度25μg/hr、*定常状態における推定平均吸収量0.6mg/日。
3). モルヒネ経口剤135~224mg/日:本剤3日貼付用量8.4mg、*定常状態における推定平均吸収速度50μg/hr、*定常状態における推定平均吸収量1.2mg/日。
4). モルヒネ経口剤225~314mg/日:本剤3日貼付用量12.6mg、*定常状態における推定平均吸収速度75μg/hr、*定常状態における推定平均吸収量1.8mg/日。
5). モルヒネ坐剤<30mg/日:本剤3日貼付用量2.1mg、*定常状態における推定平均吸収速度12.5μg/hr、*定常状態における推定平均吸収量0.3mg/日。
6). モルヒネ坐剤30~69mg/日:本剤3日貼付用量4.2mg、*定常状態における推定平均吸収速度25μg/hr、*定常状態における推定平均吸収量0.6mg/日。
7). モルヒネ坐剤70~112mg/日:本剤3日貼付用量8.4mg、*定常状態における推定平均吸収速度50μg/hr、*定常状態における推定平均吸収量1.2mg/日。
8). モルヒネ坐剤113~157mg/日:本剤3日貼付用量12.6mg、*定常状態における推定平均吸収速度75μg/hr、*定常状態における推定平均吸収量1.8mg/日。
9). モルヒネ注射剤<15mg/日:本剤3日貼付用量2.1mg、*定常状態における推定平均吸収速度12.5μg/hr、*定常状態における推定平均吸収量0.3mg/日。
10). モルヒネ注射剤15~44mg/日:本剤3日貼付用量4.2mg、*定常状態における推定平均吸収速度25μg/hr、*定常状態における推定平均吸収量0.6mg/日。
11). モルヒネ注射剤45~74mg/日:本剤3日貼付用量8.4mg、*定常状態における推定平均吸収速度50μg/hr、*定常状態における推定平均吸収量1.2mg/日。
12). モルヒネ注射剤75~104mg/日:本剤3日貼付用量12.6mg、*定常状態における推定平均吸収速度75μg/hr、*定常状態における推定平均吸収量1.8mg/日。
13). オキシコドン経口剤<30mg/日:本剤3日貼付用量2.1mg、*定常状態における推定平均吸収速度12.5μg/hr、*定常状態における推定平均吸収量0.3mg/日。
14). オキシコドン経口剤30~89mg/日:本剤3日貼付用量4.2mg、*定常状態における推定平均吸収速度25μg/hr、*定常状態における推定平均吸収量0.6mg/日。
15). オキシコドン経口剤90~149mg/日:本剤3日貼付用量8.4mg、*定常状態における推定平均吸収速度50μg/hr、*定常状態における推定平均吸収量1.2mg/日。
16). オキシコドン経口剤150~209mg/日:本剤3日貼付用量12.6mg、*定常状態における推定平均吸収速度75μg/hr、*定常状態における推定平均吸収量1.8mg/日。
17). フェンタニル注射剤<0.3mg/日:本剤3日貼付用量2.1mg、*定常状態における推定平均吸収速度12.5μg/hr、*定常状態における推定平均吸収量0.3mg/日。
18). フェンタニル注射剤0.3~0.8mg/日:本剤3日貼付用量4.2mg、*定常状態における推定平均吸収速度25μg/hr、*定常状態における推定平均吸収量0.6mg/日。
19). フェンタニル注射剤0.9~1.4mg/日:本剤3日貼付用量8.4mg、*定常状態における推定平均吸収速度50μg/hr、*定常状態における推定平均吸収量1.2mg/日。
20). フェンタニル注射剤1.5~2.0mg/日:本剤3日貼付用量12.6mg、*定常状態における推定平均吸収速度75μg/hr、*定常状態における推定平均吸収量1.8mg/日。
21). フェンタニル経皮吸収型製剤(1日貼付型製剤;フェンタニルクエン酸塩経皮吸収型製剤を含まない)貼付用量0.84mg[定常状態における推定平均吸収量0.3mg/日]:本剤3日貼付用量2.1mg、*定常状態における推定平均吸収速度12.5μg/hr、*定常状態における推定平均吸収量0.3mg/日。
22). フェンタニル経皮吸収型製剤(1日貼付型製剤;フェンタニルクエン酸塩経皮吸収型製剤を含まない)貼付用量1.7mg[定常状態における推定平均吸収量0.6mg/日]:本剤3日貼付用量4.2mg、*定常状態における推定平均吸収速度25μg/hr、*定常状態における推定平均吸収量0.6mg/日。
23). フェンタニル経皮吸収型製剤(1日貼付型製剤;フェンタニルクエン酸塩経皮吸収型製剤を含まない)貼付用量3.4mg[定常状態における推定平均吸収量1.2mg/日]:本剤3日貼付用量8.4mg、*定常状態における推定平均吸収速度50μg/hr、*定常状態における推定平均吸収量1.2mg/日。
24). フェンタニル経皮吸収型製剤(1日貼付型製剤;フェンタニルクエン酸塩経皮吸収型製剤を含まない)貼付用量5mg[定常状態における推定平均吸収量1.8mg/日]:本剤3日貼付用量12.6mg、*定常状態における推定平均吸収速度75μg/hr、*定常状態における推定平均吸収量1.8mg/日。
[換算(オピオイド鎮痛剤1日使用量に基づく推奨貼付用量):慢性疼痛における切り替え]
1). モルヒネ経口剤<45mg/日:本剤3日貼付用量2.1mg、*定常状態における推定平均吸収速度12.5μg/hr、*定常状態における推定平均吸収量0.3mg/日。
2). モルヒネ経口剤45~134mg/日:本剤3日貼付用量4.2mg、*定常状態における推定平均吸収速度25μg/hr、*定常状態における推定平均吸収量0.6mg/日。
3). モルヒネ経口剤135~224mg/日:本剤3日貼付用量8.4mg、*定常状態における推定平均吸収速度50μg/hr、*定常状態における推定平均吸収量1.2mg/日。
4). モルヒネ経口剤225~314mg/日:本剤3日貼付用量12.6mg、*定常状態における推定平均吸収速度75μg/hr、*定常状態における推定平均吸収量1.8mg/日。
5). コデイン経口剤<270mg/日:本剤3日貼付用量2.1mg、*定常状態における推定平均吸収速度12.5μg/hr、*定常状態における推定平均吸収量0.3mg/日。
6). コデイン経口剤270mg/日~:本剤3日貼付用量4.2mg、*定常状態における推定平均吸収速度25μg/hr、*定常状態における推定平均吸収量0.6mg/日。
*)本剤16.8mg(100μg/hr)は、初回貼付用量としては推奨されないが、定常状態における推定平均吸収量は2.4mg/日に相当する。
7.2. 初回貼付時
他のオピオイド鎮痛剤から本剤に初めて切り替えた場合、初回貼付24時間後までフェンタニルの血中濃度が徐々に上昇するため、鎮痛効果が得られるまで時間を要するため、次記の「使用方法例」を参考に、切り替え前に使用していたオピオイド鎮痛剤の投与を行うことが望ましい〔16.1.1-16.1.3参照〕[使用方法例]1)使用していたオピオイド鎮痛剤(経皮吸収型製剤を除く)1日1回投与:投与12時間後に本剤の貼付を開始する、2)使用していたオピオイド鎮痛剤(経皮吸収型製剤を除く)1日2~3回投与:本剤の貼付開始と同時に1回量を投与する、3)使用していたオピオイド鎮痛剤(経皮吸収型製剤を除く)1日4~6回投与:本剤の貼付開始と同時及び4~6時間後に1回量を投与する、4)使用していたオピオイド鎮痛剤(経皮吸収型製剤を除く)持続投与:本剤の貼付開始後6時間まで継続して持続投与する。
初回貼付時、患者により前記の「使用方法例」では、十分な鎮痛効果が得られない場合があるので、患者の状態を観察し、本剤の鎮痛効果が得られるまで適時オピオイド鎮痛剤の追加(レスキュー)で鎮痛を図る(1回の追加量は本剤の切り替え前に使用したオピオイド鎮痛剤が経口剤・坐剤の場合は1日量の1/6量、注射剤の場合は1/12量を目安とし、速効性のオピオイド鎮痛剤の使用が望ましい)。
7.3. 用量調整と維持
7.3.1. 疼痛増強時における処置:本剤貼付中に痛みが増強した場合や疼痛が管理されている患者で突出痛(一時的にあらわれる強い痛み)が発現した場合には、直ちにオピオイド鎮痛剤の追加投与(レスキュー)で鎮痛を図る(1回の追加量は本剤の切り替え前に使用していたオピオイド鎮痛剤が経口剤又は坐剤の場合は1日量の1/6量を、注射剤の場合は1/12量を目安とし、この場合速効性のオピオイド鎮痛剤の使用が望ましい)。
7.3.2. 増量:鎮痛効果が得られるまで各患者毎に用量調整を行うこと。鎮痛効果が十分得られない場合は、追加投与(レスキュー)されたオピオイド鎮痛剤の1日投与量及び疼痛程度を考慮し、2.1mg(12.5μg/hr)から4.2mg(25μg/hr)への増量の場合を除き、貼付用量の25~50%を目安として貼り替え時に増量する。なお、本剤の1回の貼付用量が50.4mg(300μg/hr)を超える場合で鎮痛効果が十分得られない場合は、他の方法を考慮すること。
7.3.3. 減量:連用中における急激な減量は、退薬症候があらわれることがあるので行わないこと(副作用等により減量する場合は、十分に観察を行いながら慎重に減量すること)。
7.3.4. 投与の継続:慢性疼痛患者において、本剤投与開始後4週間を経過してもなお期待する効果が得られない場合は、他の適切な治療への変更を検討し、また、定期的に症状及び効果を確認し、投与の継続の必要性について検討すること。
7.4. 投与の中止
7.4.1. 本剤の投与を必要としなくなった場合には、退薬症候の発現を防ぐために徐々に減量すること。
7.4.2. 本剤の投与を中止し、他のオピオイド鎮痛剤に変更する場合は、本剤剥離後の血中フェンタニル濃度が50%に減少するのに17時間以上かかることから、他のオピオイド鎮痛剤の投与は低用量から開始し、患者の状態を観察しながら適切な鎮痛効果が得られるまで漸増すること。
外形画像
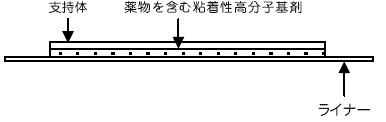
改訂情報
2025年1月6日 DSU No.332 【その他】
【11.2その他の副作用】(一部改訂)
注)増量により痛みが増悪する。
2024年3月1日 DSU No.324 【その他】
【13.過量投与】(一部改訂)
【新様式】
[症状]
フェンタニルの過量投与時の症状として、薬理作用の増強により重篤な換気低下を示す。また、フェンタニルの過量投与により白質脳症が認められている。
医師の処方により使用する医薬品。



 で医薬品を比較する
で医薬品を比較する
