ロスバスタチンOD錠5mg「JG」
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
医薬品コード(YJコード):2189017F4056
- 収載区分
- 銘柄別収載
- 先発・後発情報
- 後発品(加算対象)
- オーソライズド
ジェネリック - -
- 一般名
- ロスバスタチンカルシウム口腔内崩壊錠
- 英名(商品名)
- Rosuvastatin OD JG
- 規格
- 5mg1錠
- 薬価
- 20.60
- メーカー名
- 日本ジェネリック
- 規制区分
- -
- 長期投与制限
- -
- 標榜薬効
- 高脂血症薬〔HMG−CoA還元酵素阻害薬〕
- 色
- 薄黄
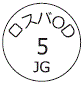
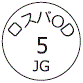
- 識別コード
- (本体)ロスバOD 5 JG (本体)ロスバOD 5 JG (被包)5 OD (被包)5 OD
- [@: メーカーロゴ]
- 添付文書
-
PDF 2024年9月改訂(第3版)
- 告示日
- 2017年12月7日
- 経過措置期限
- -
- 医薬品マスタに反映
- 2018年1月版
- DIRに反映
- 2018年1月版
- DIR削除予定
- -
- 運転注意
- 情報なし(使用の適否を判断するものではありません)
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
効能効果
高コレステロール血症、家族性高コレステロール血症。
(効能又は効果に関連する注意)
5.1. 適用の前に十分な検査を実施し、高コレステロール血症、家族性高コレステロール血症であることを確認した上で本剤の適用を考慮すること。
5.2. 家族性高コレステロール血症ホモ接合体については、LDL-アフェレーシス等の非薬物療法の補助として、あるいはそれらの治療法が実施不能な場合に本剤の適用を考慮すること。
用法用量
通常、成人にはロスバスタチンとして1日1回2.5mgより投与を開始するが、早期にLDL-コレステロール値を低下させる必要がある場合には5mgより投与を開始してもよい。なお、年齢・症状により適宜増減し、投与開始後あるいは増量後、4週以降にLDL-コレステロール値の低下が不十分な場合には、漸次10mgまで増量できる。10mgを投与してもLDL-コレステロール値の低下が十分でない、家族性高コレステロール血症患者などの重症患者に限り、さらに増量できるが、1日最大20mgまでとする。
(用法及び用量に関連する注意)
7.1. クレアチニンクリアランスが30mL/min/1.73㎡未満の患者に投与する場合には、2.5mgより投与を開始し、1日最大投与量は5mgとする〔9.2.2、9.2.3、16.6.3参照〕。
7.2. 特に20mg投与時においては腎機能に影響があらわれるおそれがあるので、20mg投与開始後12週までの間は原則、月に1回、それ以降は定期的(半年に1回等)に腎機能検査を行うなど、観察を十分に行うこと〔9.2.2、9.2.3、16.6.3参照〕。
外形画像

改訂情報
-
医師の処方により使用する医薬品。


