前回の記事では新型コロナウイルスワクチンの種類や用法用量の違いによる注意点を確認しました。
今回は国内で流通している新型コロナウイルスワクチンの有効性と副反応についてご紹介します。
新型コロナウイルスワクチンの有効性
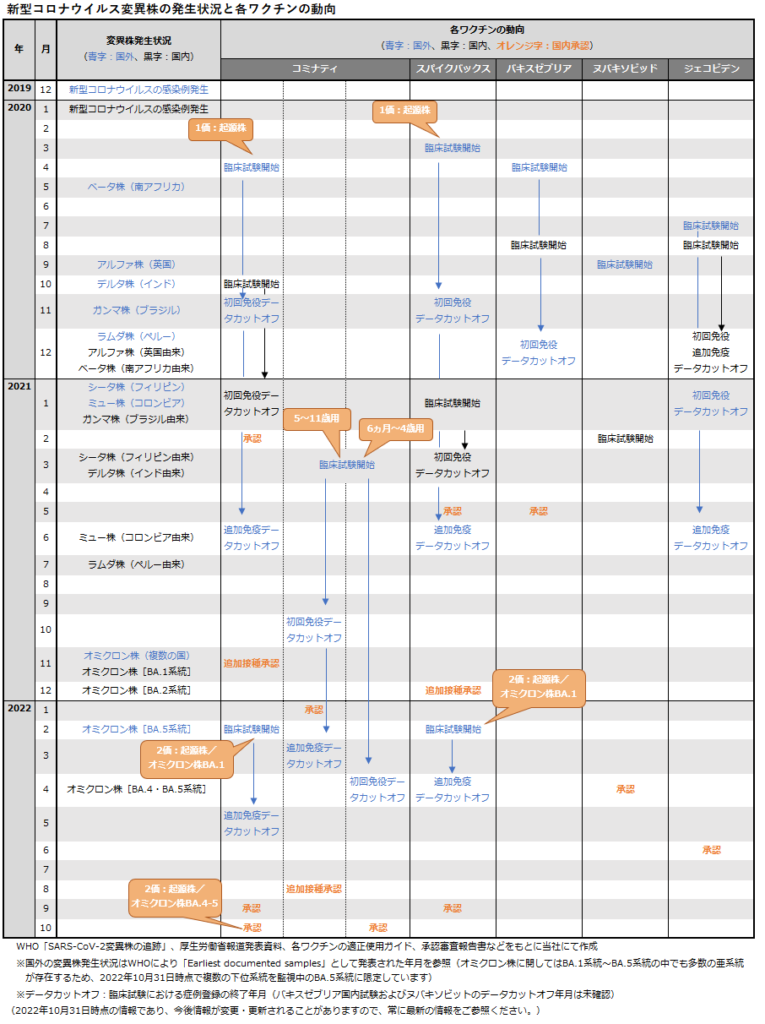
国内外における新型コロナウイルス変異株の発生状況と各ワクチンの開発状況は次のとおりです。短期間で変異が起こる新型コロナウイルスに対応するワクチンの開発が、次々と行われています。
ワクチンの有効性について考える場合、期待される予防効果と、効果を示すウイルス株を把握することが重要といえます。ワクチン接種の目的である「感染予防」「発症予防」「重症化予防」、それらの有効性の参考となる「中和抗体価」について、臨床試験のデータをもとに各ワクチンの効果をまとめました。
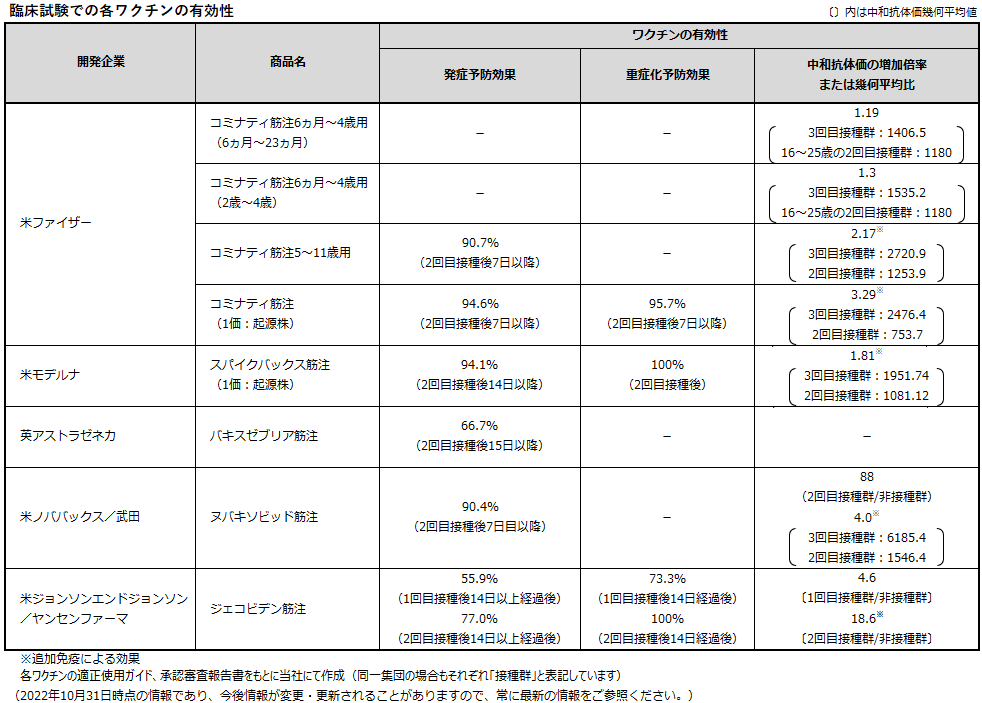
○感染予防効果:ウイルスが体内に侵入し、増えることを防ぐ効果。
○発症予防効果:風邪の様な症状や、息苦しさ、味覚障害などの各種症状が発症することを予防する効果。
○重症化予防効果:発症していても、症状が軽い・期間が短い、排出するウイルスの量が少ない・期間が短いなど、重症(集中治療室での治療や人工呼吸器等による治療などが必要な状態)に至ることを予防する効果。
○中和抗体価:ウイルスの感染力又は毒素の活性を弱める(中和する)抗体の強さで、上記の予防効果の参考指標。中和抗体価が高い方が発症予防効果は高い。
コミナティ筋注(1価:起源株)、スパイスバックス筋注(1価:起源株)、バキスゼブリア筋注については、海外の研究において、次表の通り発症予防効果と重症化予防効果が報告されています。
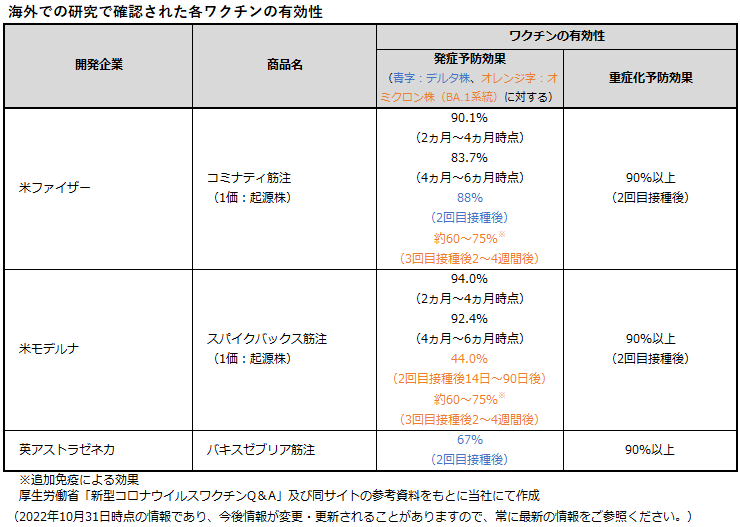
新型コロナウイルスワクチンは、一般に感染予防効果も期待されていますが、数値化された報告は研究段階のため、今後も情報を注視していく必要があります。
発症予防効果は時間の経過とともに徐々に低下しますが、重症化予防効果は発症予防効果に比べ、時間が経過しても比較的高く保つことができると報告されています。
また、どのワクチンでも追加免疫により中和抗体価が増加していることが分かります。ただし、現段階では不明確な点も多く、長期的なワクチンの持続効果については、引き続き最新の情報を注視する必要があります。
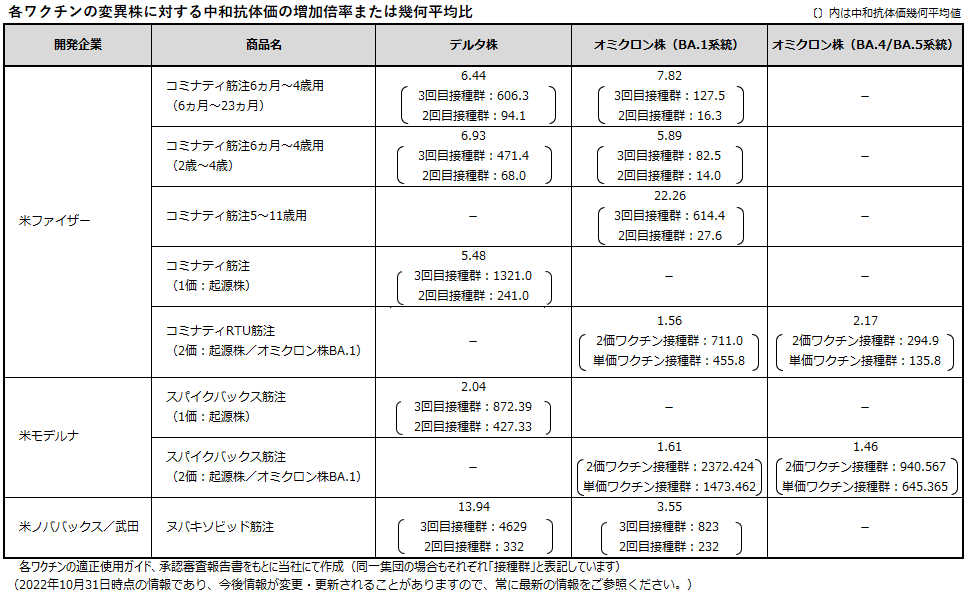
変異株に対する中和抗体価について下表にまとめました。オミクロン株に対する中和抗体価はデルタ株と比較して低く、初回免役獲得後の持続時間が短いと報告されています。上表と照らし合わせても発症予防効果はデルタ株と比較して低いことが分かります。ただし、追加免疫により一時的に効果が回復することが分かっています。
ワクチン接種後に発現する副反応
新型コロナウイルスワクチン接種後の主な副反応(注射部位疼痛、発熱、疲労、頭痛)の発現頻度についてまとめました。
添付文書における各ワクチンの主な副反応の発現頻度は以下の図の通りです。
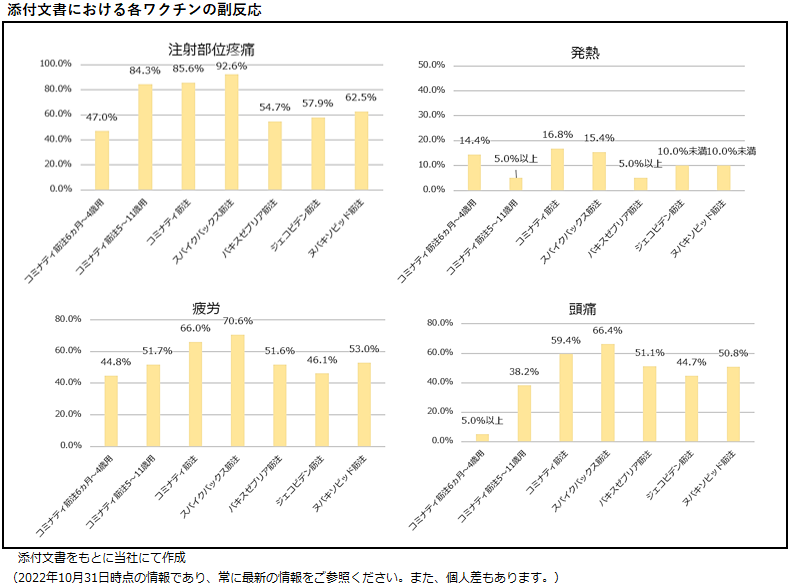
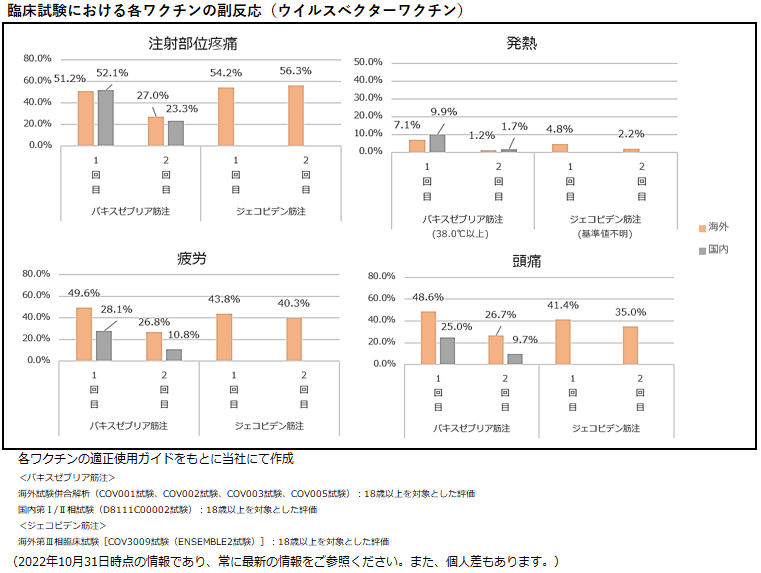
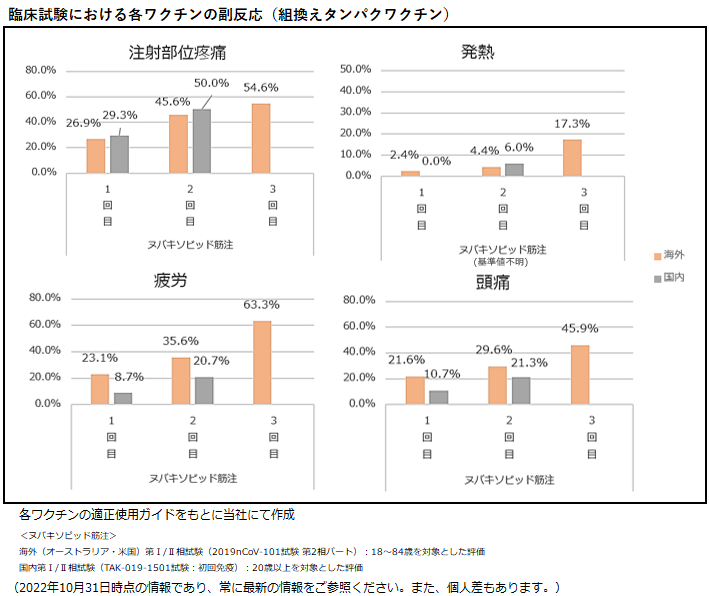
添付文書には統合された情報が記載されていますが、臨床試験では各ワクチンで接種回数ごとに異なる発現頻度の副反応が報告されています。以下は、各ワクチンの適正使用ガイドに掲載された臨床試験の情報をもとに副反応の発現頻度をワクチンのタイプごとにまとめた図です。追加免疫においては、2022年10月31日時点で国内での試験結果が公表されていないため、海外での試験結果のみを参照しています。
また、新型コロナウイルスワクチン接種後の副反応は、年代によっても異なることが報告されています。本来は各年代別で比較すべきですが、各ワクチンにおける臨床試験被験者の年代構成が異なるため、単純比較が難しい点ご留意ください。
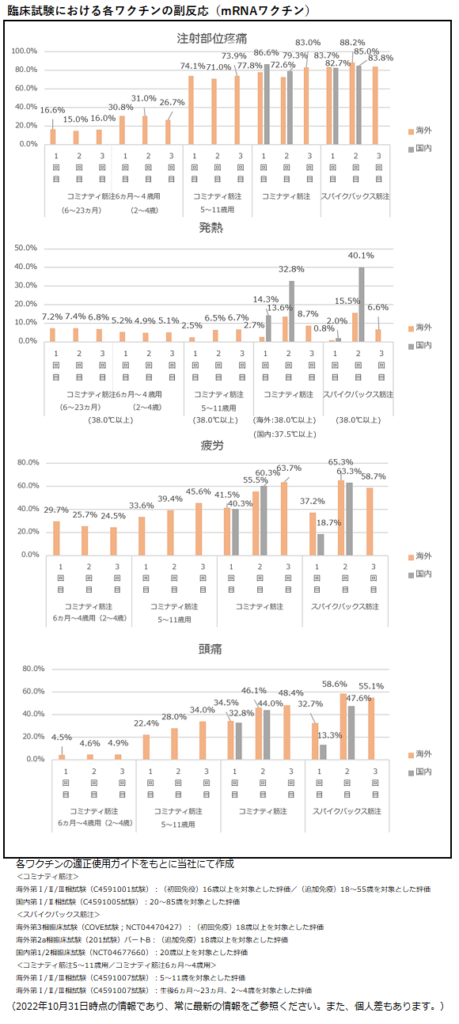
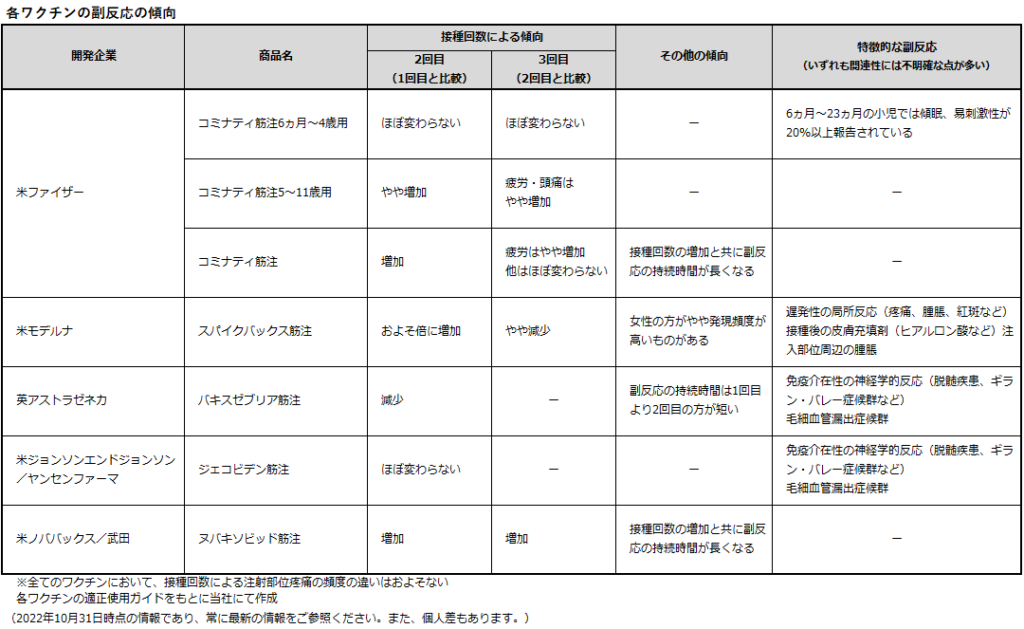
mRNAワクチンであるコミナティ筋注やスパイクバックス筋注では、初回よりも2回目接種時に副反応の発現頻度が高くなり、3回目以降は1価、2価に関わらず、ほとんど変わらないかやや減少する傾向にあります。また、発熱の発現頻度は海外と国内の臨床試験で大きな差が出ています。
ウイルスベクターワクチンでは注射部位疼痛、発熱、疲労の発現の割合がmRNAワクチンよりも低く、特にバキスゼブリア筋注は、初回よりも2回目接種の方が、発現頻度が低くなっています。
組換えタンパクワクチンではいずれの副反応についても接種回数を重ねる方が、頻度が上がる傾向があります。
その他の傾向としては、スパイクバックス筋注は、男性より女性の方が副反応の発現頻度が全体的に高いことが確認されています。
各ワクチンの接種回数ごとの副反応の頻度と、報告されている特徴的な副反応を下表にまとめました。
ワクチン接種後に発現する重篤な副反応
国内での新型コロナウイルスワクチン接種後に発現した重篤な有害事象として、アナフィラキシー、心筋炎、心膜炎について、次の件数が報告されています。
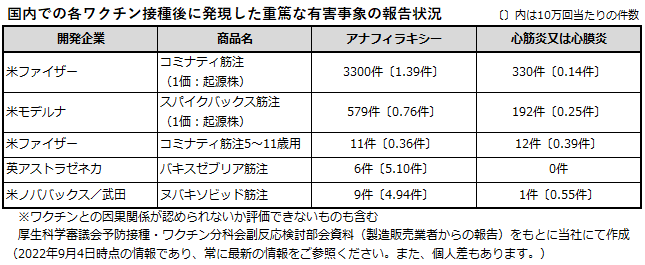
アナフィラキシーは新型コロナウイルスワクチンに限定して起こる事象ではなく、風邪薬やその他のワクチンでも発現する可能性があります。例えば、インフルエンザワクチン接種後の副反応疑い報告では、ワクチンとの因果関係が認められないか評価できないものも含めて、1シーズンで約20件の事例が報告されています。新型コロナウイルスワクチンの接種会場や医療機関には、アナフィラキシーに対応できる医薬品が準備されています。アナフィラキシーは接種後30分以内に発現することが多いため、問診内容によって接種会場で30分間待機することで対策が取られています。
心筋炎や心膜炎はmRNAワクチンにおいて発現が確認されている副反応です。10代及び20代の男性が、他の年代と比べて発現頻度が高い傾向が確認されています。胸の痛みや息切れなどの症状に、特に接種後4日程度の間、注意する必要があります。
新型コロナウイルス関連医薬品の各種情報を「薬の検索」からご確認いただけます
二回にわたり新型コロナウイルスの各ワクチンについて紹介してきました。公表されているデータをもとに、様々な要素について一覧化するために比較を試みていますが、製薬企業ごとの表現の違いや、各ワクチンの臨床試験・研究の諸条件の差異のため、単純に比較することは困難であり、本記事の各図表は見やすさに重点を置いた参考情報であることをご承知おきください。
ワクチンを取り巻く環境はいまだ急速に変化しています。次々と新たな変異株が発生しており、ワクチン接種の対象年齢や投与間隔などの用法もそれにあわせて短期間に更新されています。今後も変異株の発生状況と新型コロナウイルスワクチンの動向を注視すると共に、適切な情報を確認していくことが大切です。
―参考資料―
コミナティ筋注(1価:起源株) 添付文書(2022年10月改訂:第19版)
スパイクバックス筋注(1価:起源株) 添付文書(2022年10月改訂:第16版)
バキスゼブリア筋注 添付文書(2022年8月改訂:第6版)
コミナティ筋注5~11歳用 添付文書(2022年9月改訂:第5版)
コミナティ筋注6ヵ月~4歳用 添付文書(2022年10月作成:第1版)
ヌバキソビッド筋注 添付文書(2022年10月改訂:第6版)
ジェコビデン筋注 添付文書(2022年6月作成:第1版)
コミナティRTU筋注(2価:起源株/オミクロン株BA.1) 添付文書(2022年10月改訂:第2版)
スパイクバックス筋注(2価:起源株/オミクロン株BA.1) 添付文書(2022年9月改訂:第2版)
コミナティRTU筋注(2価:起源株/オミクロン株BA.4-5) 添付文書(2022年10月改訂:第2版)
コミナティ筋注・コミナティ筋注5~11歳用・コミナティ筋注6ヵ月~4歳用(1価:起源株) 適正使用ガイド(2022年10月作成版)
スパイクバックス筋注(1価:起源株) 適正使用ガイド(2022年8月作成版)
バキスゼブリア筋注 適正使用ガイド(2022年5月作成版)
ヌバキソビッド筋注 適正使用ガイド(2022年9月作成版)
ジェコビデン筋注 適正使用ガイド(2022年6月作成版)
コミナティRTU筋注(2価:起源株/オミクロン株) 適正使用ガイド(2022年10月作成版)
スパイクバックス筋注(2価:起源株/オミクロン株BA.1) 適正使用ガイド(2022年9月作成版)
厚生労働省 新型コロナワクチンQ&A
https://www.cov19-vaccine.mhlw.go.jp/qa/0011.html
N Engl J Med. 2021;385:585-594.
Lancet.2021;S0140-6736(21)00947-8
N Engl J Med 2021; 385:1774-1785
N Engl J Med 2021 Sep
N Engl J Med 2021; 385:1761-1773
https://www.cov19-vaccine.mhlw.go.jp/qa/0111.html
COVID-19 vaccine surveillance report Week 16 UK Health Security Agency 2022/4/21
https://www.cov19-vaccine.mhlw.go.jp/qa/column/0001.html
https://www.cov19-vaccine.mhlw.go.jp/qa/0079.html
https://www.cov19-vaccine.mhlw.go.jp/qa/0005.html
厚生労働省 新型コロナウイルス感染症の“いま”に関する11の知識(2022年10月版)
https://www.mhlw.go.jp/content/000927280.pdf
PMDA コミナティ筋注(1価:起源株)の審査報告書
https://www.pmda.go.jp/drugs/2021/P20210212001/672212000_30300AMX00231_A100_6.pdf
https://www.pmda.go.jp/drugs/2021/P20211108001/672212000_30300AMX00231_A100_2.pdf
PMDA スパイクバックス筋注(1価:起源株)の審査報告書
https://www.pmda.go.jp/drugs/2021/P20210519003/400256000_30300AMX00266_A100_4.pdf
https://www.pmda.go.jp/drugs/2021/P20211213004/400256000_30300AMX00266_A100_2.pdf
PMDA バキスゼブリア筋注の審査報告書
https://www.pmda.go.jp/drugs/2021/P20210519002/670227000_30300AMX00267_A100_4.pdf
PMDA コミナティ筋注5~11歳用の審査報告書
https://www.pmda.go.jp/drugs/2022/P20220117002/672212000_30400AMX00015000_A100_2.pdf
https://www.pmda.go.jp/drugs/2022/P20220826003/672212000_30400AMX00015_A100_1.pdf
PMDA ヌバキソビッド筋注の審査報告書
https://www.pmda.go.jp/drugs/2022/P20220415001/400256000_30400AMX00192_A100_2.pdf
PMDA ジェコビデン筋注の審査報告書
https://www.pmda.go.jp/drugs/2022/P20220617001/800155000_30400AMX00203000_A100_1.pdf
PMDA コミナティRTU筋注(2価:起源株/オミクロン株BA.1)の審査報告書
https://www.pmda.go.jp/drugs/2022/P20220912001/672212000_30400AMX00016_A100_1.pdf
PMDA スパイクバックス筋注(2価:起源株/オミクロン株BA.1)の審査報告書
https://www.pmda.go.jp/drugs/2022/P20220912003/790314000_30300AMX00461_A100_1.pdf
PMDA コミナティ筋注6ヵ月~4歳用の審査報告書
https://www.pmda.go.jp/drugs/2022/P20220926003/672212000_30400AMX00438_A100_2.pdf
厚生労働省 新型コロナウイルス感染症に関する報道発表資料
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000121431_00086.html
WHO SARS-CoV-2変異株の追跡
https://www.who.int/en/activities/tracking-SARS-CoV-2-variants/
厚生労働省 第85回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第14回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)
https://www.mhlw.go.jp/stf/shingi2/0000208910_00052.html




