※この記事は2019年3月以前の記載要領に沿った添付文書情報を対象としています。
医薬品の添付文書における各項目に記載されている情報について、読み解きます。
はじめに、【警告】の項に記載されている情報について読み解きます。
【警告】の項の情報を読み解く
【警告】の情報がある場合、添付文書はこのような形式で記載されています。
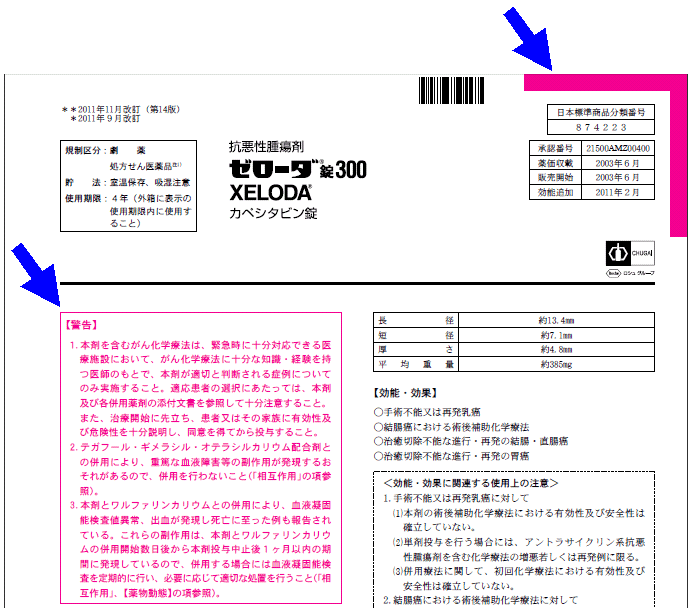
しかし、【警告】の情報であっても、すべてが“禁忌”とは限りません。
例に挙げた、ゼローダ錠300の【警告】情報を読み解きます。
1.の情報…がん化学療法の施行、および本剤を使用する場合の患者さんの同意取得について、注意を喚起する内容が記載されています。
2.の情報…本剤とテガフール・ギメラシル・オテラシルカリウム配合剤との併用が禁忌である旨が記載されています。
3.の情報…本剤とワルファリンカリウムとの併用が注意である旨が記載されています。
このように、【警告】の情報であっても、ゼローダ錠300を使用するにあたり、禁忌であることと注意を要するが可能なことの情報が記載されています。
「【警告】の項に記載されているのだから、ゼローダ錠300とワルファリンカリウムとの併用は禁忌なのではないか?」とのご質問をよく頂きますが、添付文書の記載内容を読み解くと、『出血が発現して死亡に至った例も報告されているので、血液凝固能検査を定期的に行うなどの注意は必要だが、併用は可能』となります。
以上のように、【警告】の項に記載されている情報がすべて【禁忌】とは限らないということを、承知しておく必要があります。
次に、【相互作用】の項に記載されている情報について読み解きます。
【相互作用】の項の情報を読み解く
【相互作用】の相手薬剤の記載パターン
【相互作用】の項における相手薬剤に関する情報は、大きく分けて次の4つのパターンで記載されています。
(1)具体的な成分名(一般名)のみが記載されているパターン

(2)“○○系薬剤”や“△△阻害剤”のように薬効とその薬効における代表的な成分名(一般名)が記載され、その他は『等』としてまとめられているパターン

(3)“○○系薬剤”や”△△阻害剤”のように薬効とその薬効に属する成分名(一般名)が記載されているが、『等』の表記がないパターン

(4)作用とその作用を有する薬剤について、薬効とその薬効における代表的な成分名(一般名)で記載されているパターン

(1)のパターンは、相手薬剤の成分名(一般名)のみがズバリ記載されているので明解です。
しかし、(2)、(3)、(4)のパターンは、相手薬剤の対象範囲について判断を迷う記載です。
【相互作用】の相手薬剤の情報を読み解く
『等』の記載の有無
上記(2)と(3)のパターンを比較すると、薬効とその薬効に属する成分名(一般名)が記載されているところまでは同じですが、『等』の有無に違いがみられます。
『等』の記載があるパターン(2)の場合は、機序を参照しても同じ薬効の薬すべてが対象と判読できます。
一方、『等』の記載がないパターン(3)の場合は、記載されている成分の薬だけが対象と判読すべき場合と、同じ薬効の薬すべてが対象と判読すべき場合があることにご留意ください。その判読基準として、機序の欄に記載されている情報を参考にすることをお奨めします。
作用の記載
次にパターン(4)の場合ですが、このように『作用』と『その強弱』であったり、“QT延長を起こすことが知られている薬剤”というような『認知』による記載の場合は、情報の読み手側にその判読基準が委ねられています。
更に、上述したように『等』の有無も考慮する必要があります。
また、(4)の例に示した“CYP3A4”といった肝薬物代謝酵素とその関連薬剤については、網羅・整理された情報が乏しく調査検討の難しさに拍車をかけているのが現状です。
これらの問題への対処方法としては、日々の情報収集と安全性を重視しつつ治療を妨げることのない視点が重要です。
相互作用に関する情報の記載項目
相互作用に関する情報は、【相互作用】の項に記載されているのが原則です。
しかし、医薬品によっては相互作用に関する情報を確認する際に、その記載項目に十分注意を払う必要があります。
下記のとおり、ウテメリン錠5mgの添付文書における【慎重投与】の(7)には、カリウム減少性利尿剤の投与を受けている患者さんに対しては慎重に投与する必要がある旨の注意が記載されています。

ところが、【相互作用】の項において、カリウム減少性利尿剤との併用に関して注意が必要であるという情報が記載されていません。

このように、本来【相互作用】に記載されるべき情報であっても、【相互作用】以外の項にしか記載がない場合があります。
このことから、相互作用に関する情報を添付文書から得ようとする場合、【相互作用】の項だけではなく他の項目についても情報を確認すべきであるという認識を持つ必要があります。
最後に、【副作用】の項に記載されている情報について読み解きます。
【副作用】の情報を読み解く
副作用関連情報の記載項目
副作用に関する情報は、【副作用】の項における“重大な副作用”、もしくは“その他の副作用”に記載されているのが原則です。
しかし、次のように添付文書の後半にある【その他】の項にも記載されています。
(1)評価の確立していない文献、報告であっても重要な情報は要約して記載
(2)いずれの項にも属さない安全性を確保する上で必要な情報、例えば動物での毒性試験結果等が記載

従って、副作用情報を検索する際はこのような点にも留意し、情報を見落とさないようにする必要があります。
【副作用】の表記について
添付文書では、記載のレイアウトについては規定されていますが、記載する情報の表現までは規定されていません。
従って、次のような副作用の表記が行われていることがあります。
(1)平仮名と漢字による両方の表記が同一添付文書上に記載されているパターン
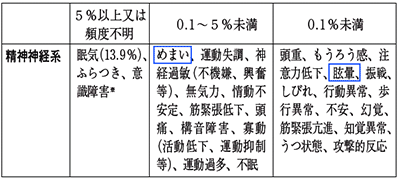
(2)漢字(日本語)表記とカタカナ(英語)による表記のばらつきがあるパターン

情報を検索する際は、このような“表記のゆれ”についても考慮をしなければ検索の漏れが生じ、臨床における安全性の確保に支障を来たす恐れがありますので、十分に留意する必要があります。




